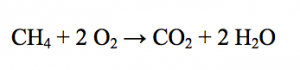Physique-Chimie
L'organisation et la structure de la matière en chimie en 3ème
Au collège, même si les sciences physiques occupent une plage horaire restreinte, elles permettent de donner aux élèves une culture scientifique pour d'aborder des sujets de notre époque (écologie, énergie, développement durable...) avec comme moteur, la curiosité.
Les transformations chimiques
C'est à travers d'autres types de transformations chimiques telles que celles :
- entre les acides et les bases (au cours desquelles des dégagements gazeux se produisent),
- entre les acides et les métaux,
que votre enfant apprend à identifier d'autres espèces chimiques telles que les ions (avec des banques de tests fournies).
La compréhension de ce que sont les ions passe par un travail sur la structure de l'atome. L'aspect historique présente un grand intérêt car il montre que les connaissances dans ce domaine sont récentes; n'hésitez pas à aller voir !
La présence de certains ions peut être détectée par des tests simples et cette étape est souvent appréciée des élèves car ils se rendent compte qu'ils travaillent comme des « vrais » chimistes. On peut pousser l'exercice en leur confiant une enquête à mener, avec des liquides à identifier pour connaître l'auteur d'un crime imaginaire…
Parmi les ions étudiés, figurent ceux responsables de l'acidité ou la basicité des liquides. On peut ainsi quantifier le caractère acide ou basique du jus de citron, d'un soda ou d'une lessive avec du papier pH ou un pH-mètre.
|
|
|
Basique, c'est à dire de pH > 7 (lessive St Marc, destop…).
Acide signifie pH ‹ 7 (jus citron, vinaigre, coca...).
Un liquide est soit acide, soit basique.
Si son pH = 7, il est neutre (eau, savons).
Ces mesures ont des applications bien concrètes lorsqu'il s'agit de contrôler la qualité de l'eau d'une piscine, d'un aquarium ou d'un sol pour choisir les plantations qui y sont adaptées. Il est alors indispensable de sensibiliser les élèves sur le fait que certaines solutions présentent un réel danger du fait de leur basicité ou leur acidité (on n'utilise pas du Destop sans gants et lunettes…) et qu'il y a des réflexes à adopter en cas d'incident.
Les acides sont capables d'attaquer certains métaux dont le fer. Cette attaque impressionnante fait l'objet d'un chapitre de synthèse dans lequel toutes les connaissances acquises sont réutilisées (tests d'ions, test explosif du dihydrogène…).
Ces réactions ne sont pas à reproduire du fait de leur dangerosité et les mises en garde ne doivent pas être prises à la légère, comme en témoigne l'article suivant.
Les équations chimiques
Utiliser une équation de réaction chimique pour décrire une transformation chimique est un des objectifs à atteindre à la fin du cycle de chimie.
Il suffit de s'assurer que les atomes présents dans les produits (formés) soient de même nature et en même nombre que dans les réactifs, c'est-à-dire les molécules présentes au départ.
Par exemple, il devra comprendre que la combustion du carbone se traduit par :
Et celle du combustion du méthane par: